Perhatikan tabel pengisian elektronelektron berikut! Uns...

Perhatikan tabel pengisian elektronelektron ke dalam sub...
Elektron - Wikipedia Bahasa Melayu, ensiklopedia bebas. Elektron adalah satu zarah subatom keunsuran berjisim ringan yang membawa cas negatif cas elektrik. Elektron mempunyai spin 1/2 ( fermion ), tidak terlibat di dalam salingtindak kuat ( lepton) dan tidak mempunyai substruktur.

Perhatikan konfigurasi elektron unsur dan Y berikut! Jika...
Konfigurasi elektron dituliskan berdasarkan aturan yang telah disepakati oleh ilmuan-ilmuan terkemuka. Aturan-aturan dalam penulisan konfigurasi elektron antara lain yaitu prinsip aufbau, kaidah hund, larangan pauli, serta hukum mekanika kuantum.

Pengisian Elektron Yang Benar Ditunjukkan Oleh Unsur Berbagai Unsur
Jawaban terverifikasi. Pembahasan. Prinsip aufbau menyatakan bahwa elektron menempati suatu orbital dengan urutan peningkatan energi tertentu. Urutan energi berdasarkan aufbau mengikuti urutan berikut: 1s<2s<2p<3s<3p<4s<3d<4p<5s<4d<5p<6s<4f<5d<6p<7s<5f<6d<7p.

Pengisian elektron pada orbital yang benar adalah.
Pada modul ini akan dipelajari bagaimana memperkiran bentuk molekul suatu senyawa dengan menggunakan teori Valence Shell Electron Pair of Repulsion (VSEPR) dan Teori Domain Elektron dan mengaitkan dengan sifat fisik suatu senyawa terutama titik didih/titik leleh. Download Free PDF. View PDF.

BELAJAR KIMIA PENYIMPANGAN PENGISIAN KONFIGURASI ELEKTRON YouTube
Berdasarkan pengertian diatas dapat dijelaskan bahwa terdapat dua cara dalam suatu penulisan konfigurasi elektron. Cara tersebut yaitu bisa berdasarkan kulit atom atau berdasarkan subkulit atomnya. Konfigurasi elektron ini berdasarkan kulit atom hanya berlaku untuk unsur golongan utama, yaitu unsur golongan IA sampai VIIIA.

Konfigurasi Elektron Dalam Orbital Untuk Unsur 18Ar Adalah Ujian
Pembahasan. Pengisian elektron harus berlandaskan prinsip aufbau dan aturan hund yaitu: Prinsip Aufbau, pengisian elektron dimulai dari sub kulit yang memiliki tingkat energi rendah menuju tingkat energi yang tinggi.

Diagram lintasan elektron unsur P dengan nomor atom = 15
Struktur Atom dan Tabel Periodik. Konfigurasi Elektron dan Diagram Orbital. Perhatikan tabel pengisian elektron-elektron dalam subkulit berikut! Unsur Pengisian Elektron 7 3 Li 1s^2 2s^1 11 5 B 1s^2 2s^2 3s^1 23 11 Na 1s^2 2s^2 2p^6 3s^1 27 13 AI 1s^2 2s^2 2p^6 3s^2 3p^3 56 26 Fe 1s^2 2s^2 2p^6 3s^2 3p^6 4s^1 3d^5 Pengisian elektron yang benar.

Cara Cepat Menuliskan Konfigurasi Elektron, Golongan, dan Periode YouTube
Unsur-unsur yang memilikistruktur elektron terluar (elektron valensi) yang sama ditempatkan pada golongan (kolom) yang sama. Dengan demikian, unsur-unsur yang segolongan memiliki sifat-sifat kimia yang sama.

Pengisian Elektron Yang Benar Ditunjukkan Oleh Unsur Berbagai Unsur
Uns. Perhatikan tabel pengisian elektron-elektron berikut! Unsur Pengisian Elektron 1 1s^2 2s^2 2p^5 2 1s^2 2s^2 2p^5 3s^2 3 1s^2 2s^2 2p^6 3s^1 3p^1 4 1s^2 2s^2 2p^6 3s^2 3p^4 4s^1 5 1s^2 2s^2 2p^6 3s^2 3p^6 4s^2 3d^5 Pengisian elektron yang benar menurut aturan Aufbau dan Hund adalah unsur.

pengisian elektron yang benar ditunjukan oleh unsur.... Brainly.co.id
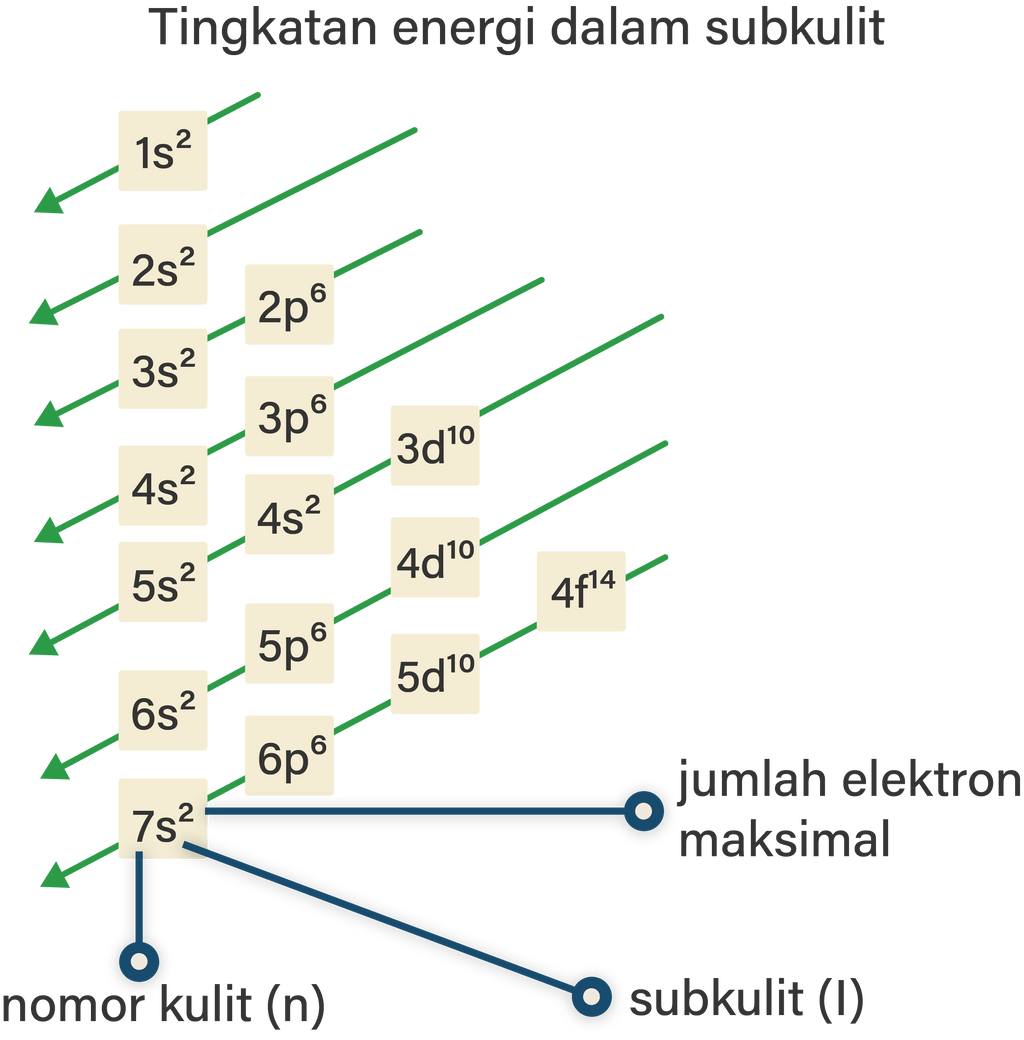
Prinsip Aufbau. Prinsip ini menyatakan bahwa pengisian elektron dimulai dari tingkat energi terendah menuju tingkat energi yang lebih tinggi. Bila digambarkan maka sebagai berikut: Beberapa kaidah yang harus diikuti dalam penentuannya adalah. Urutan pengisian orbital mengacu pada arah urutan panah, yaitu 1s, 2s, 2p, 3s, 3p dan sterusnya. b.

Gambarkan Konfigurasi Elektron Untuk Atom Netral
Berdasarkan perspektif Bohr, elektron harus diisi dari tingkat energi paling rendah ke tinggi, yaitu secara berurutan mulai dari kulit K (n=1), L (n=2), M (n=3), N (n=4) dan seterusnya. Untuk jumlah elektron maksimal pada lapisan kulit dihitung berdasarkan rumus , dengan penjelasan n = nomor kulit. 2. Konfigurasi Elektron Subkulit.

Konfigurasi Elektron Dan Cara Menuliskannya
"Pengisian elektron dalam orbital dimulai dari orbital dengan tingkat energi paling rendah. Setelah penuh, pengisian berlanjut ke orbital yang tingakat energinyas atu tingkat lebih tinggi. Demikian seterusnya hingga semua elektron menempati orbital." Aturan Aufbau. Urutan pengisian elektron pada orbital dari tingkat energi yang terendah adalah:

Molekul Unsur Dan Senyawa Secara Berurutan Lengkap
Berdasarkan teori ini, elektron harus diisikan dari tingkat energi paling rendah, yaitu kulit K ( n = 1) dan dilanjutkan kulit L ( n = 2), M ( n = 3), N ( n = 4), dan seterusnya. Banyaknya elektron yang mengisi setiap kulit mengikuti rumus 2 n2. Dengan demikian: Kulit K = 2 n2 = 2 (1) 2 = 2 elektron maksimal.

Pengisian Elektron Yang Benar Ditunjukkan Oleh Unsur Berbagai Unsur
Konfigurasi elektron adalah susunan atau gambaran yang menunjukan penempatan elektron dalam suatu atom. Susunan elektron-elektron tersebut berdasarkan kulit atau orbital. Konfigurasi elektron dalam atom, bisa diungkapkan dengan diagram curah hujan dan diagram orbital.
Video belajar Pengisian Elektron Pada Orbital Kimia untuk Kelas 10 IPA
Urutan energi berdasarkan aufbau mengikuti urutan berikut: 1s<2s<2p<3s<3p<4s<3d<4p<5s<4d<5p<6s<4f<5d<6p<7s<5f<6d<7p. Subkulit s: maksimal diisi 2 elektron. Subkulit p: maksimal diisi 6 elektron. Subkulit s: maksimal diisi 10 elektron. Subkulit s: maksimal diisi 14 elektron.
Jelaskan tentang konfigurasi elektron beserta cont...
Subkulit 1s punya tingkat energi paling rendah, lalu naik ke subkulit 2s, 2p, 3s, 3p, sampai terakhir yang paling tinggi 8s. Pastinya elektron yang bisa mengisi subkulit tertentu juga terbatas. Elektron yang mengisi subkulit ini dituliskan dalam bentuk pangkat.